El CMCiB rep el certificat de compliment de bones pràctiques de laboratori (BPL) en recerca preclínica
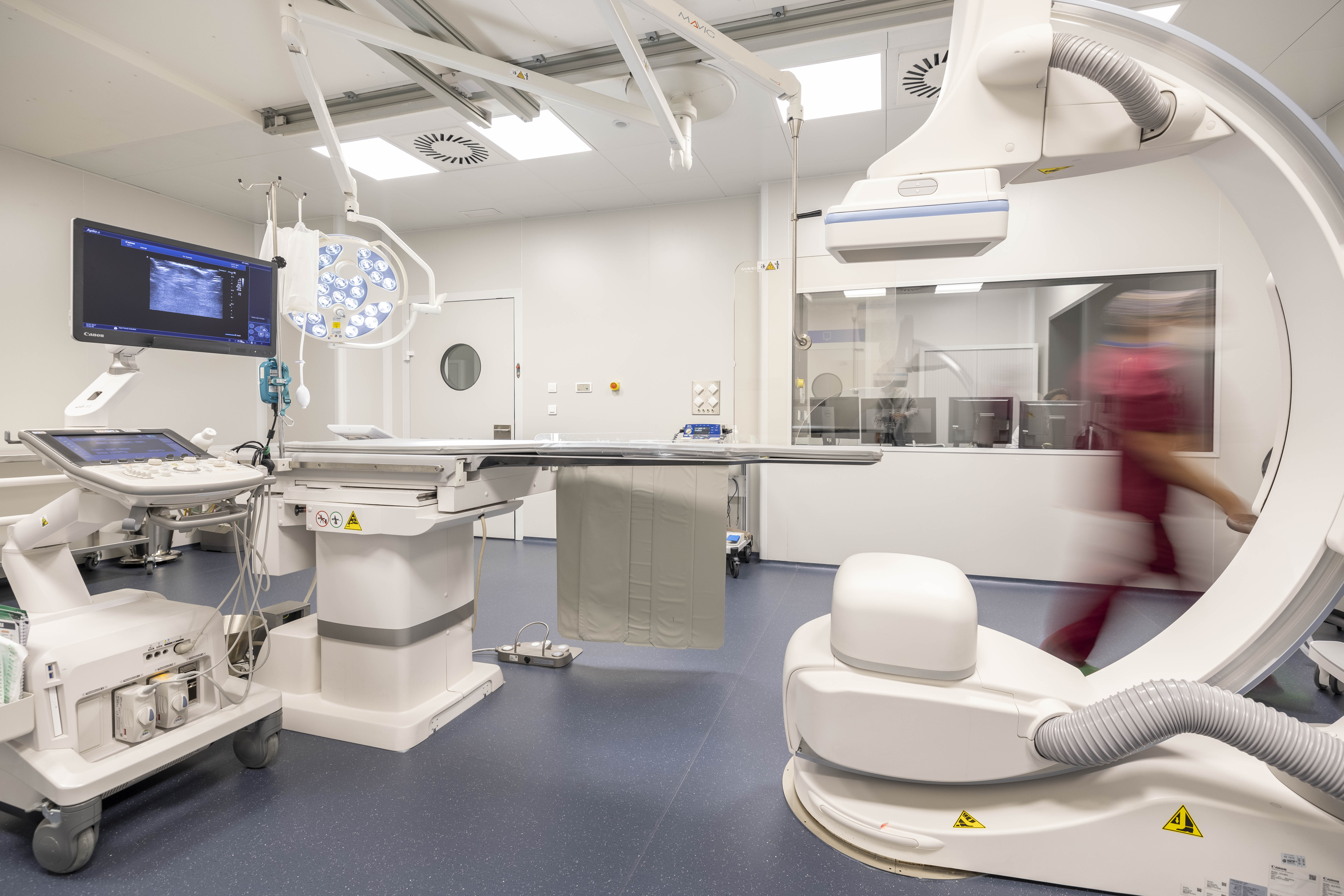
El Centre de Medicina Comparativa i Bioimatge (CMCiB) de l'Institut de Recerca Germans Trias i Pujol (IGTP) ha rebut el certificat de compliment de bones pràctiques de laboratori (BPL) d'acord amb la Directiva 2004/9/CE. El centre compleix els principis establerts al Reial decret 822/19932 en la realització d'estudis preclínics amb productes sanitaris (proves analítiques i de química clínica -hematologia i bioquímica- en estudis d'administració de producte d'assaig i obtenció d'espècimens i biocompatibilitat de productes sanitaris). L'àrea quirúrgica i de bioimatge, incloses les tecnologies de radiologia vascular intervencionista, ecografia i ressonància magnètica, són les que s'han certificat.
Aquest certificat, atorgat per la Generalitat de Catalunya, garanteix la qualitat i la integritat dels resultats dels laboratoris de recerca que duen a terme estudis preclínics. Així mateix, aquesta fita normativa mostra l'adhesió del CMCiB als estàndards internacionals de recerca. Des de l'any 2021, la legislació demana que els dispositius mèdics -com poden ser les pròtesis, catèters, vàlvules, stents, cirurgies, etc.- estiguin validats preclínicament sota aquesta certificació BPL abans d'iniciar assajos clínics.
Per assolir aquesta certificació, el CMCiB ha incorporat tres professionals més de l'àmbit del control de qualitat al seu equip i ha comptat amb el suport de la Unitat de Garantia de Qualitat de FalcoQuality, que ha fet la formació del personal en els principis de les BPL, l'assessorament en tot el procés d'implantació i duu a terme totes les activitats del programa de garantia de qualitat. L'equip de professionals del CMCiB ha estat treballant durant l'últim any i mig per a la implantació del sistema de qualitat. La certificació obtinguda ajuda a posicionar el CMCiB-IGTP com a centre de referència per a la realització d'estudis preclínics de dispositius mèdics en les condicions exigides per les agències reguladores, ajudant a les empreses en el procés de portar aquest tipus de productes al mercat.
*
Bones pràctiques de laboratori (BPL)
Els principis de bones pràctiques de laboratori (BPL) configuren un sistema de qualitat relatiu a l'organització i les condicions en què els laboratoris de recerca planifiquen, duen a terme, controlen, registren i arxiven els estudis no clínics de seguretat sanitària i mediambiental sobre substàncies i productes químics. Aquests estudis són necessaris per poder registrar i/o autoritzar productes químics com a medicaments, tant d'ús humà com veterinari, productes cosmètics, productes sanitaris, plaguicides, fitosanitaris, additius destinats a l'alimentació humana i animal i substàncies químiques industrials.
A Catalunya i des de l'any 1995, l'organisme encarregat de vetllar pel compliment dels principis de BPL en els estudis sobre seguretat sanitària i ambiental de medicaments, productes sanitaris establerts per l'Organització per a la Cooperació i Desenvolupament Econòmic (OCDE) i la Unió Europea, és el Departament de Salut de la Generalitat de Catalunya. Concretament, el Servei de Control Farmacèutic i Productes Sanitaris de la Direcció General d'Ordenació i Regulació Sanitària.
El CMCiB és un centre tecnològic que dona suport a la recerca biomèdica en els àmbits de la cirurgia, el diagnòstic per la imatge, les malalties infeccioses i l'oncologia principalment. Utilitza models animals quan és necessari tot promocionant la recerca responsable a través del programa 3R, que incorpora l'ús del peix zebra i la mosca drosòfila, les modelitzacions matemàtiques, la bioimatge i els programes de benestar animal.
